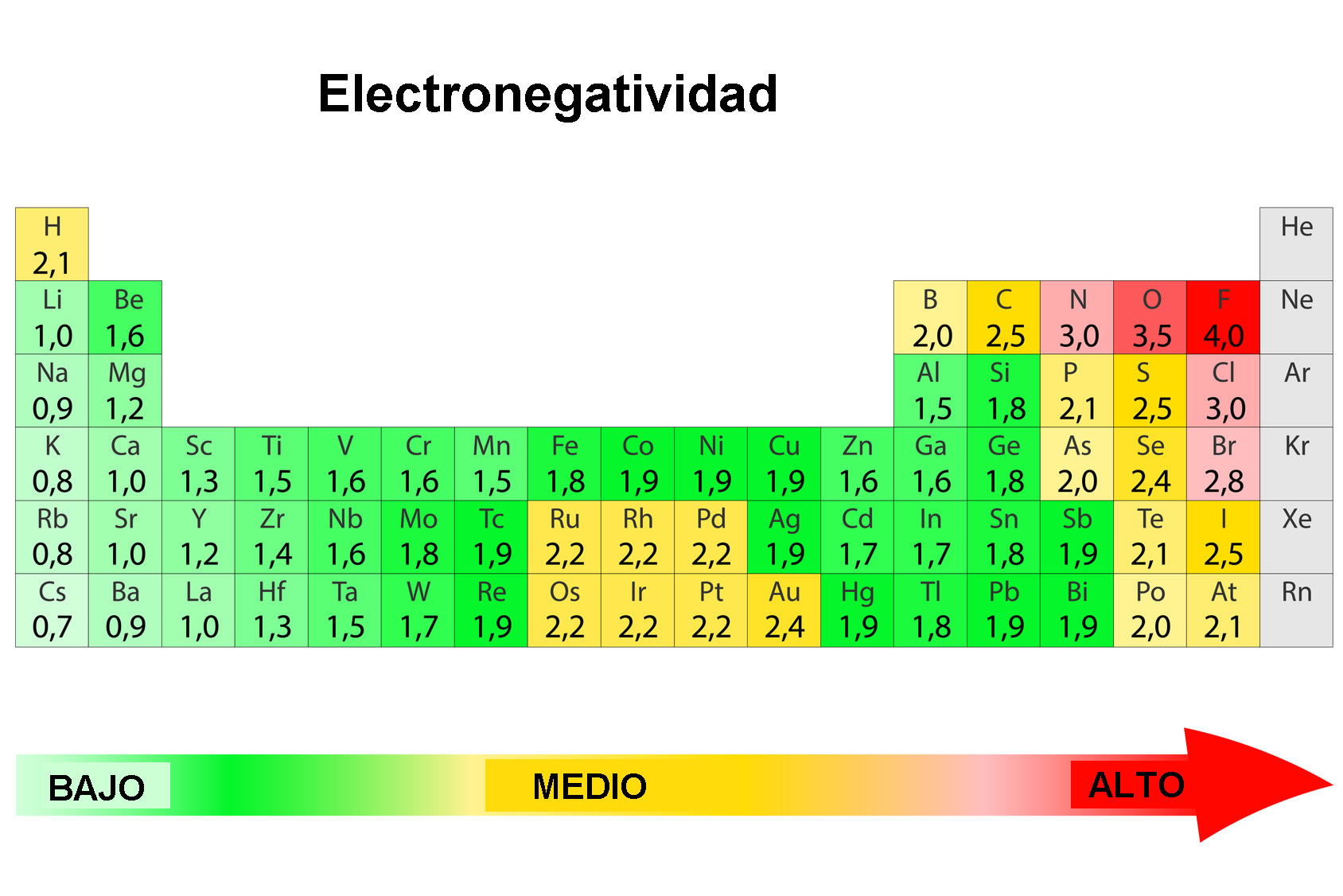
Los átomos tienen la capacidad de atraer hacia ellos los diferentes pares de electrones que, a su vez, están unidos con otros átomos conectados por un enlace químico. La medición de dicha capacidad es conocida como electronegatividad.
En otras palabras, este fenómeno se produce cuando dos átomos diferentes comparten dos electrones. Este concepto adquiere sentido únicamente cuando nos referimos a átomos enlazados.
A través del mismo podemos establecer qué tipo de enlace se producirá en los diferentes tipos de átomos.
A través de esta propiedad podemos comprender mejor la reactividad de las moléculas
Si un átomo x tiene una electronegatividad mayor que la de un átomo y, los electrones no se sitúan en el centro de ambos, sino que están más próximos al átomo x. Esta reacción provoca que la molécula no sea totalmente simétrica en su polaridad, sino que en una parte tiene una carga negativa y en otra una carga positiva. Por el contrario, si la electronegatividad de los dos átomos es similar, los electrones que se comparten estarían más unidos (en este caso no se producen cargas parciales y se trataría de una molécula apolar, es decir, sin polaridad).
La escala de Pauling
En el ámbito de la química se emplea una escala de electronegatividad basada en valores de energías de enlace de diferentes moléculas y conocida como la escala de Pauling. Sus magnitudes van de 0. 7 a 4. Así, los átomos menos electronegativos presentan un valor de 0.7 y son el cesio y el francio, mientras que el valor 4 lo tiene el flúor, el elemento más electronegativo de la tabla periódica.
Como consecuencia de ello, si combinamos un elemento con mucha electronegatividad con otro con una elevada electropositividad, el primero tendrá una cantidad mayor de electrones que el segundo. Por ejemplo, en una molécula de fluoruro de cesio los átomos son muy diferentes, pues el flúor tiene el valor máximo y el cesio el valor mínimo (en este caso los electrones se encuentran más próximos al flúor).
Otras propiedades de los átomos
Al margen de la electronegatividad, los átomos tienen otras propiedades físicas y químicas. De esta manera, para diferenciar unos átomos de otros es necesario determinar su número atómico y su número másico.
El número atómico se define como el número de protones que están presentes en el núcleo y número másico se define como la cantidad de partículas que están presentes en el núcleo, es decir, la suma del número de protones más el número neutrones.
Por otra parte, los átomos son estudiados por su tamaño, su potencial de ionización y su afinidad electrónica.
